باتری های لیتیومی
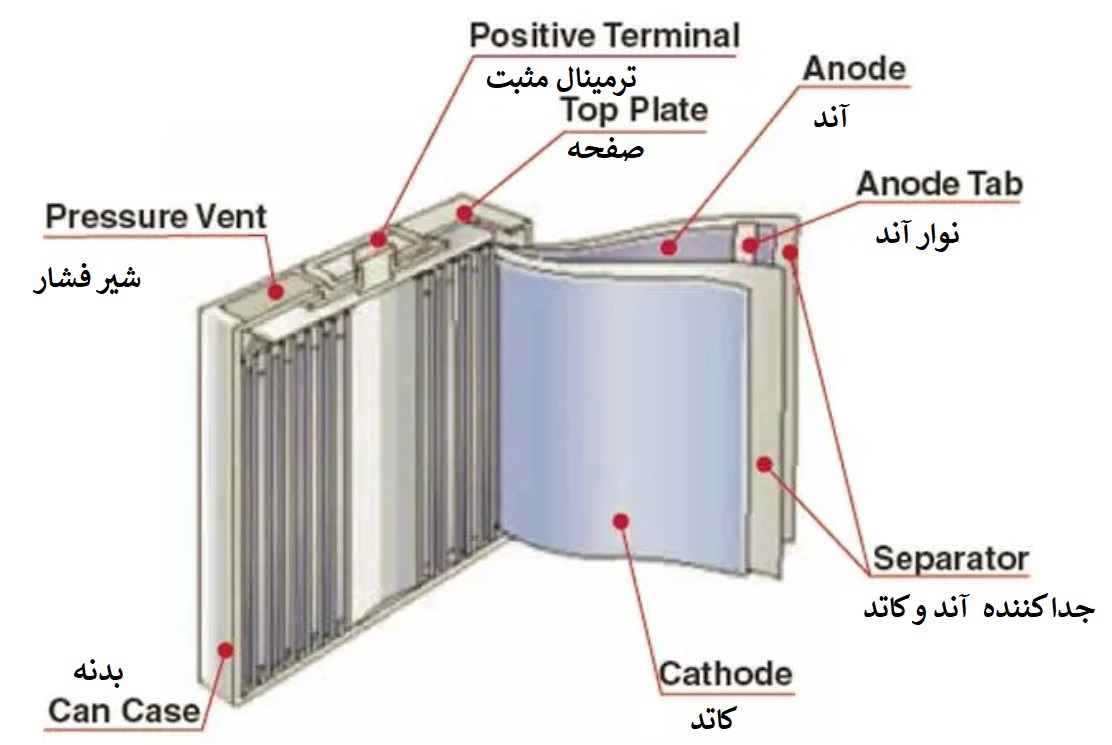
باتریهای یون لیتیومی از سه بخش درست شدهاند. الکترود مثبت و منفی و الکترولیت.
معمولاً جنس الکترود منفی از کربن و جنس الکترود مثبت از اکسید فلزی است. الکترولیت نمک لیتیم در یک حلال ترکیب آلی است.
به صورت تجاری جنس الکترود منفی (کاتد) از گرافیت است. جنس الکترود مثبت(آند) یکی از مادههای زیر است: یک لایه ای از اکسید (مثل لیتیم کبالت اکسید)، پلی آنیون مثل (لیتیم آهن فسفات) یا یک لعل مثل منگنز اکسید.
عموماً الکترولیت مخلوطی از ترکیبات آلی کربنی مثل اتیلن کربنات یا دیاتیل کربنات که شامل کمپلکس شیمیایی یونهای لیتیم است، میباشد. این الکترولیتها که معمولاً در آب حل نمیشوند و محلول آبی تشکیل نمیدهند عموماً از نمکهای آنیون غیر هماهنگ مثل لیتیوم هگزافلوئوروفسفات (LiPF6)، لیتیوم هگزافلوئوروآرسنات مونوهیدرات (LiAsF6)، لیتیوم پرکلرات (LiClO4)، لیتیوم تترافلوئوروبورات (LiBF4) و لیتیوم تری فلات (LiCF3SO3) استفاده میکنند.
بسته به نوع مواد استفاده شده در باتریهای لیتیمی، ولتاژ، چگالی انرژی، طول عمر و ایمنی بهطور قابل توجهی میتواند تغییر کند. در حال حاضر تلاشها برای بهبود عملکرد این باتریها با استفاده از نانوفناوری ادامه دارد. حوضههایی که روی این موضوع کار میکنند: مواد مورد استفاده در الکترودها در مقیاس نانو و دیگر ساختارهای جایگزین الکترود میباشد.
لیتیم خالص واکنشپذیری (شیمی) بسیار بالایی دارد. این ماده با آب شدیداً واکنش نشان میدهد و به شکل لیتیم هیدروکسید (LiOH) و گاز هیدروژن در میآید. به همین خاطر از موادی برای الکترولیت استفاده میکنند که در آب حل نمیشود و محفظه باتری برای اینکه رطوبت رو به خودش جذب نکند عایق کاری میشود.
باتریهای لیتیمی نسبت به باتریهای نیکل–کادمیم بسیار گرانتر هستند اما در رنج گرمای بیشتری کار میکنند و چگالی انرژی بیشتری دارند. این باتریها نیاز به مدار محافظ دارند تا ولتاژ پیک رو کنترل کنند.
در صورتی باتری بیش از حد تخلیه شود یا بیش از حد شارژ شود باتری خراب میشود. به همین منظور از مدار محافظ الکترونیکی در باتریها استفاده میشود. این مدار را شما حتی روی باتریهای قدیمی گوشیهای قدیمی نیز میتوانید ببینید.